محتويات
علم الكيمياء
هو أحد العلوم الطبيعيّة والتي تشمل على علوم الأرض، علم الفلك وعلم الأحياء، ويعد فرعًا من فروع العلوم الفيزيائيّة، وهو العلم الذي يدرس المادة والتغيّرات التي تطرأ على خواصها، بنيتها، تركيبها، سلوكها، تفاعلاتها وتداخلاتها التي تحدثها، ويدرس الكيمياء الذّرات والرّوابط التي تحدث بينها مكونةً الجزيئات، ويُعدُّ جابر بن حيان الملقّب بأبي الكيمياء المؤسّس الحقيقي لعلم الكيمياء، وتعتبر للكيمياء أهميةً كبيرةً في حياتنا فهي تدخل في مختلف المجالات كالصّناعات الدّوائيّة، الغذاء، الدّهان، الأسلحة وغيرها، وتنقسم الكيمياء إلى فروعٍ عدةٍ تتفرّع منها أقسام أخرى، أهمها: الكيمياء العامّة والتي تدرس المبادئ الأساسيّة في الكيمياء، والكيمياء العضويّة وتهتم بدراسة المواد العضويّة، والكيمياء التحليليّة كالتحليل الكهربائي البسيط، فما هو تعريف التحليل الكهربائي البسيط؟[١]
تعريف التحليل الكهربائي البسيط
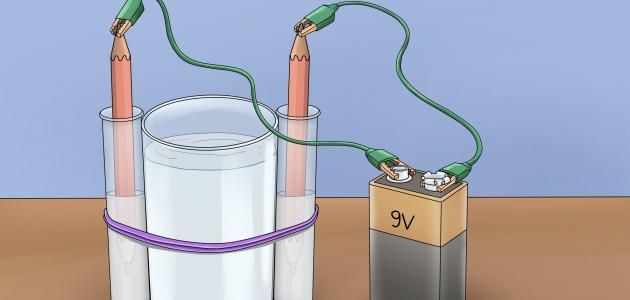
يتم تعريف التحليل الكهربائي البسيط على أنه الطريقة التي يتم بها استخدام تيار كهربائي لإطلاق تفاعل كيميائي، ويحدث بواسطة خلية التحليل الكهربائي وهي بمثابة جهاز يتم فيه تحويل الطاقة الكهربائية إلى طاقة كيميائية أو العكس، وللتحليل الكهربائي أهمية تجارية كبيرة؛ فهو يسهل عملية فصل العناصر من أشكالها الموجودة في الطبيعة مثل الفلزات، كما يستخدم في تحضير المواد التي يصعب تحضيرها بالوسائل الكيميائيّة أو بسبب ارتفاع تكاليف الطرق الكيميائية لإنتاجها، كتحضير الألمونيوم، ومحلول هيدروكسيد الصوديوم النقي.[٢]، ولفهم التحليل الكهربائي للخلية أكثر، يجب معرفة ما يأتي:
مكونات خليلة التحليل الكهربائي
تتكون خلية التحليل الكهربائي عادةً من قطبين موصلين معدنين أو إلكترونين تسمى بالأقطاب الكهربائية، وتكون هذه الأقطاب معزولة عن بعضها البعض ضمن محلول كهرلي أي موصلٍ للكهرباء، عند مرور تيارٍ كهربائيٍّ بين القطبين فإنه يجعل أحدهما مشحونًا بشحنة سالبة والآخر مشحونًا بشحنة موجبة، تهاجر الأيونات الموجبة في المحلول إلى القطب السّالب والذي يعرف بالكاثود وهناك تتّحد مع إلكترون واحد أو أكثر، وتفقد جزءًا أو كلًا من شحنتها وتصبح أيونات جديدة ذات شحنةٍ منخفضةٍ أو ذراتٍ أو جزيئاتٍ محايدة، في نفس الوقت تهاجر الأيونات السّالبة إلى القطب الموجب وهو الأنود وتنقل إلكترونًا واحدًا أو أكثر إليه، وتصبح أيضًا أيونات جديدة أو جزيئات محايدة، والتّأثير الكلي للعمليتين هو نقل الإلكترونات من الأيونات السّالبة إلى الأيونات الموجبة، أي عن طريق التحليل الكهربائي يحدث انفصالًا للنّواتج.[٣]
طريقة انتقال الأيونات في المحلول الكهرلي
يتم انتقال الأيونات في المحلول عن طريق النفاذيّة في المحلول وعن طريق قوى التجاذب الكهروستاتيكي بين الأيونات والأقطاب، وتحتاج هذه العملية لفرق جهدٍ معينٍ ويسمى جهد التّحلل، ويجب أن يكون فرق الجهد مساويًا لجهد التّحلل أو يزيد عنه لكي تحدث عملية التحليل، وإذا كان فرق الجهد أقل من الحد المطلوب فلا تتم العملية، ويصبح سطح كل قطب ملامس للمحلول غير موصل للكهرباء.[٤]
الكيمياء التحليلية
بعد تعريف التحليل الكهربائي البسيط، والذي يعد جزءًا من الكيمياء التحليليّة، لذلك سيتم توضيح ما هي الكيمياء التحليليّة؛ إذ تعرف بأنّها العلم الذي يبحث في تحليل المكونات الكيميائيّة للعينات المدروسة، أي تحليل عينات من المادة لمعرفة التركيب الكيميائي لها وكيفيّة بنائها، وتستخدم الكيمياء التحليليّة طرق تحليل تقليديّة أو آليّة، ويتم استخدامها والّلجوء إليها في جميع الفروع والأنواع الأخرى للكيمياء، وتقسم إلى قسمين:[١]
- التّحليل النّوعي: يهتم بالكشف عن العناصر الكيميائية أو المجموعات الوظيفيّة أو المركبات الكيميائيّة دون الإهتمام بكمية المادة أو نسبتها، والتي تتحدد بوسائل التّحليل الكمّي.[٥]
- التّحليل الكمّي: ويستخدم بتحديد كمية ونسبة كل عنصر من العناصر أو الأيونات الدّاخلة في تركيب العينة، ويعطي هذا النوع من التّحليل بياناتٍ أكثر دقةٍ عن تكوين عينةٍ ما والمكونات التي تدخل في تكوينها ومقاديرها، وهو نوعان: حجمي ووزني.[٥]
المراجع[+]
- ^ أ ب "What Is Chemistry?", www.livescience.com, Retrieved 15-07-2019. Edited.
- ↑ "Electrolysis: Definition, Types & Uses", study.com, Retrieved 15-07-2019. Edited.
- ↑ "Electrolytic cell", www.britannica.com, Retrieved 15-07-2019. Edited.
- ↑ "Electrolysis", chem.libretexts.org, Retrieved 15-07-2019. Edited.
- ^ أ ب "Analytical chemistry", en.wikipedia.org, Retrieved 15-07-2019. Edited.